
人类自然杀伤细胞(Nature Killer Cell,NK)占所有循环淋巴细胞的15%。NK细胞发现于20世纪70年代,主要与杀死感染的微生物和恶性转化的同种异体和自体细胞有关。
NK细胞来源于CD34+共淋巴祖细胞。据估计,NK细胞的半衰期大约为7~10天,它占人类外周血淋巴细胞总数的10-15%,也存在于脾脏、肝脏、肺、骨髓和淋巴结中,它们通过与DC细胞的相互作用发挥关键的免疫调节功能。
NK细胞是第一组固有淋巴样细胞的典型成员,具有分泌 IFN-γ 的能力。
终末分化的 NK 细胞缺乏B淋巴细胞(CD19-)和 T 淋巴细胞(CD3-)的表型标记,CD56是NK细胞特征的标志。
人外周血NK细胞可分为CD56bright和CD56dim两大类。 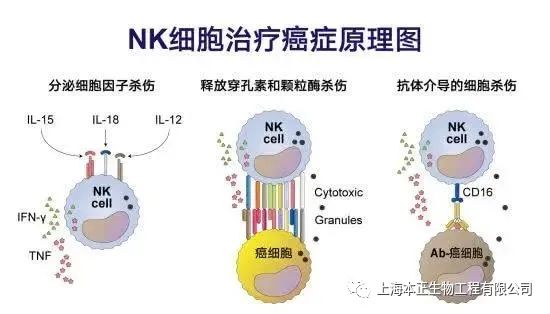
1、NK细胞疗法概述
CAR-T细胞免疫治疗技术发展迅速,但在临床应用中仍存在一些不足,例如在实体瘤的治疗中显示出很低的疗效;不同的患者对CAR-T治疗的耐受力有着很大的差别,部分患者会产生不同程度的神经毒性和细胞因子风暴。
这也是CAR-T治疗致力于改善的一个方向。
自然杀伤细胞(Nature Killer ),成为一个充满潜力的候选疗法。
1975年,Kiessling等人给出了NK 细胞的基本定义。NK细胞来源非常广泛,比如外周血、脐带血、胚胎干细胞、人类诱导多能干细胞和NK细胞系。

细胞因子风暴(CRS)是由CAR-T细胞分泌的INF-γ、TGF-α、IL-1和IL-6因子等诱导的。然而,NK细胞分泌IL-3和GM-CSF,因此不太可能引起CRS。
由于肿瘤微环境中PD-1的表达,CAR-T细胞的功能受到抑制。NK细胞分泌的PD-1水平较低,免疫抑制作用较小,这使NK细胞成为抗实体瘤的理想候选细胞。
此外,NK细胞促进DC细胞迁移到肿瘤中,从而增强抗PD-1免疫治疗。
NK细胞对肿瘤细胞具有一定的杀伤效果,而且不受MHC识别的限制,是肿瘤免疫治疗的潜在治疗方式。
异体来源NK细胞几乎不会诱发移植物抗宿主病(GVHD),不会导致CRS,可以作为完全“现货型”产品使用。
在临床前和临床试验中,CAR-NK细胞疗法当之无愧成为细胞疗法中的热门选手。
2、CAR-NK细胞概述
CAR(嵌合抗原受体)技术是基因工程与免疫疗法的完美融合,是当前肿瘤治疗领域最具前景的研究方向之一。 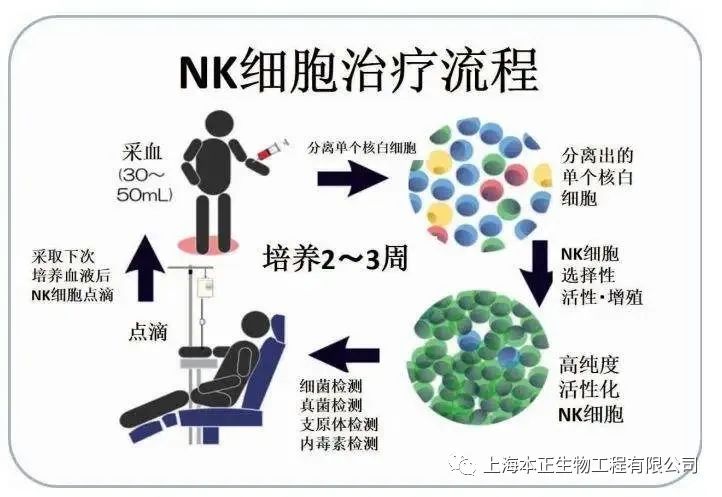
CAR-NK细胞,由识别肿瘤特异抗原的细胞外信号结构域、跨膜区和细胞内结构域组成,它们可以建立新的激活途径,以增强靶细胞的溶解。
CAR-NK细胞,不仅通过CAR特异性识别抗原表达肿瘤的能力,而且通过NK细胞受体自身来消除肿瘤。
NK细胞的活性取决于是刺激和抑制信号的平衡,而不是抗原特异性。这些信号激活衔接蛋白,释放穿孔素和颗粒酶,并控制细胞因子的产生。
NK细胞的另一种杀伤机制,涉及抗体依赖性细胞介导的细胞毒性。因此,CAR-NK细胞的靶向裂解基于CAR依赖和NK受体依赖机制,并且裂解也适用于抗原阴性膜的肿瘤。
3、CAR-NK细胞疗法的研究现状
NK细胞的临床前试验,证明了其在造血干细胞治疗后对AML的临床治疗能力。
然而,肿瘤逃避免疫监视,NK细胞的临床治愈率也不高,因此限制了它们的治疗前景。
CAR修饰被认为是NK细胞提高细胞毒性的一种策略。
最近,CAR修饰的NK细胞在肿瘤中的作用正在被广泛研究。 
根据clinical.gov网站上的临床数据,已有200多项关于CAR-T细胞的研究。
然而,有9项涉及CAR-NK细胞。
4、临床应用障碍和应对策略
CAR-NK细胞疗法的改进
迄今为止,CAR-NK细胞疗法进行了广泛的临床前研究。
患者源性肿瘤异种移植(PDX)模型,是临床癌症的优秀模型,因为它直接将肿瘤从患者转移到NSG或NOG小鼠。
大多数CAR-NK细胞疗法在临床前试验中已在PDX模型中进行了疗效评估,包括针对血液瘤靶点(如CD19、CD20、CD138和CS-1)和实体瘤(如HER2、GD2、PSCA和EGFRvIII)。
与PDX相比,人源化小鼠更为精确。通过将干细胞回输到免疫缺陷小鼠体内以使其发育人类免疫系统,克服了PDX模型未能观察到CAR-NK/T对肿瘤微环境中宿主免疫细胞影响的失败。 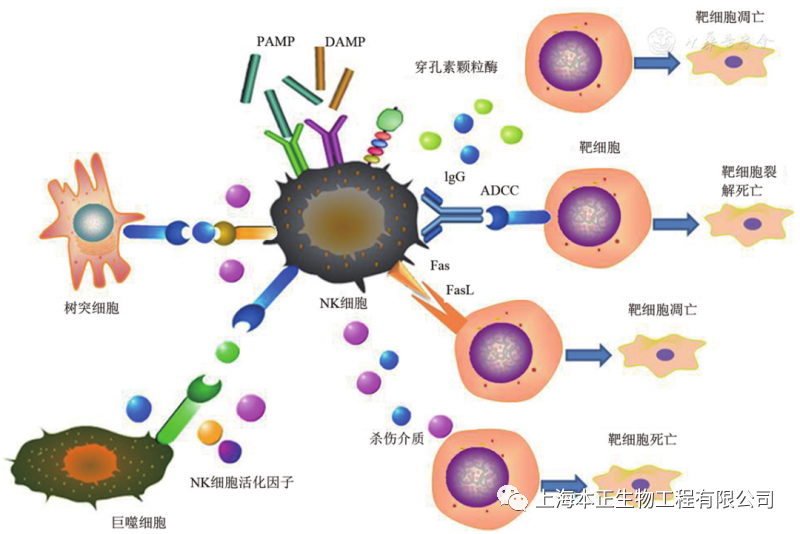
临床应用障碍和应对策略
CAR-NK细胞疗法具有巨大的潜力,但需要解决一些基本问题,以扩大其临床应用。
首先,NK细胞体外培养扩增是第一道障碍。单个供体的NK细胞数量不足以进行治疗,这使得NK细胞的扩增和激活变得非常关键。通常需要两到三周来培养NK细胞。
供体细胞数量的可用性仍然是一个障碍。此外,必须完全清除T细胞,以防止GVHD。
因此,如何获得足够的NK细胞仍是一个挑战。
第二,选择合适CAR很关键。目前的CARs是为构建CAR-T细胞而设计的。
因此,对于NK细胞来说,是次优的选择。CAR结合表位的位置及其与CAR-NK细胞表面的距离影响其结合抗原和激活CAR-NK细胞的能力。
第三,选择合适的方法将CAR转化到NK细胞是CAR-NK细胞免疫治疗的关键。
到目前为止,病毒载体和非病毒载体都被用来转化CAR。
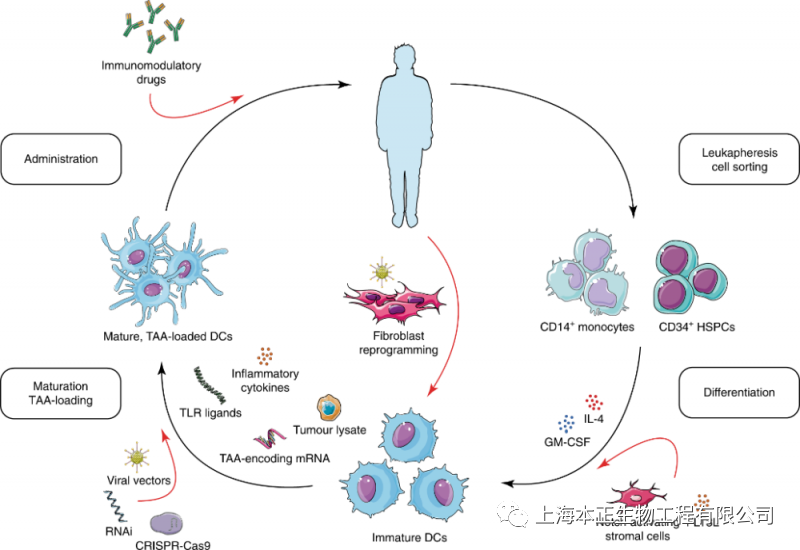
虽然逆转录病毒载体的转染效率很高,但它可能会引起插入突变、致癌和其他不良反应。而慢病毒载体尽管显示出较低的插入突变发生率,但其对外周血NK细胞的转染效率低至20%。
睡美人系统已成功应用于CAR-T。然而,它对CAR-NK结构的适用性尚不清楚。mRNA转染CAR-NK细胞也被认为是一种安全、实用的转染方法。
最后,NK细胞对冻融过程敏感。解冻后NK细胞的存活率和细胞毒性显著降低。
一些研究小组发现,加入IL-2可以部分恢复冷冻NK细胞的活性。为了使细胞冷冻保存成为可行的最佳策略,必须对冷冻NK细胞进行探索。
5、安全性和有效性提高的新策略
CAR-NK细胞疗法的安全性
将自杀基因整合到CARs和双特异性CARs中可以提高CAR-NK细胞治疗的安全性。 
HSV-TK/GCV自杀系统在20世纪90年代首次用于干细胞治疗。凋亡途径,如Fas和caspase9已经被利用。
CAR掩蔽肽由阻断抗原结合位点的掩蔽肽和蛋白酶结合点组成。当蛋白酶裂解连接从TME中的掩蔽肽分离时,CAR-T细胞可以在肿瘤局部保持活性。
将HIF1的氧敏感域与CAR结构融合,设计了氧敏感CAR。此外,CAR-T被设计成当synNotch和CAR配体在肿瘤上共同表达时激活,这是一种在空间上识别并有效控制CAR-T细胞激活的策略。
此外,临床治疗正在进行,以评估抗CD19/CD22(NCT03448393)和抗CD19/CD20(NCT03271515)的双特异性CAR-T细胞治疗的疗效,以防止抗原丢失引起的复发。
CAR-NK细胞疗法的有效性 
在设计CAR-NK细胞的过程中,沉默NK抑制受体使其对肿瘤有更强的抵抗力。
当IL-4和IL-7受体结构域与反向细胞因子受体(4/7 ICR)融合并添加到CAR构建物中时,一些研究组发现来源于肿瘤的IL-4抑制作用降低,促进了CAR-T细胞的增殖。
转染CAR/ICR的T细胞在体内对含IL-4的TME具有持续的抗肿瘤作用。考虑到CAR-NK细胞的特异性,ICR受体(IL-15,IL-21)是否适用于CAR-NK细胞,尚需进一步研究。
有趣的是,CAR-T/NK细胞维持着固有的代谢过程。以4-1BB作为共刺激分子的CAR-NK细胞依赖于氧化代谢,增强线粒体活性、NK细胞增殖和持久性,并增强抗PD-1活性。
因此,可以尝试通过调节CAR-T/NK细胞的代谢来提高疗效。
6、文末小结
NK 细胞具有独特的抗肿瘤效应,不受MHC限制的细胞毒性、产生细胞因子和免疫记忆等功能,使其成为先天性和适应性免疫反应系统中的关键角色。
CAR-NK 细胞疗法是一个很有前途的临床研究领域,对某些癌症患者具有良好的安全性和初步疗效。相信,CAR-NK细胞疗法可能会导致肿瘤免疫治疗的革命性进展。
上海本正生物工程有限公司提供的干细胞是从脐带、胎盘中提取的一种修复器官机理的未完全分化的原始细胞,具有自我更新、多项分化和高度繁殖的能力,医学上称为“万能细胞”,它是形成人体各种组织器官的起源细胞。干细胞对临床上一些疑难疾病的治疗如:脑瘫、老年痴呆、脑萎缩、帕金森病、中风、肝硬化、糖尿病、红斑狼疮、股骨头坏死、软骨和关节损伤、心脏和脊髓损伤等,取得显著效果,它拥有更加鲜活细胞能量,可以快速、有效进入体内,分泌多种有益细胞因子,调节体内微环境,激活干细胞再生能力,重启时光之门,追溯青春绽放源头,实现对人体衰老状态减缓,同时有效改善身体亚健康以及预防肿瘤发生。

|
