
我国是肝癌大国,世界卫生组织国际癌症研究机构(IARC)2020年最新全球癌症数据显示:我国肝癌新发病例41万例,肝癌死亡病例39万例。近7成肝癌患者发现时都已经是中晚期,生存期很短,如果不治疗只进行护理,平均寿命只有三个月到半年时间。
为什么大多数肝癌发现就是晚期?
最主要的原因是肝脏的代偿功能太强大。人类的肝脏有左右两个叶,主要由肝细胞组成。当然它还有其他类型的细胞,包括排列在血管上的细胞和排列在肝脏中称为胆管小管子上的细胞。
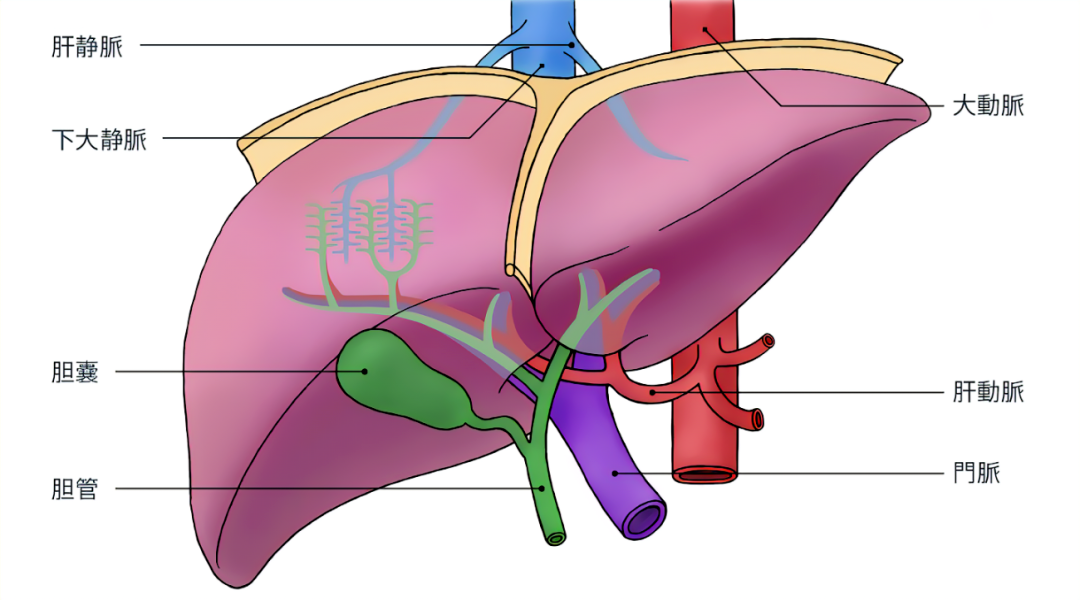
肝门静脉和肝动脉使得肝脏具有全身器官中独有的双重血液供应――大约20%的血供来自肝动脉,80%来自门静脉。门静脉收集自腹腔流来的血液,血中的有害物质及微生物抗原性物质,将在肝内被解毒和清除。因此肝脏也被称为是人体的解毒器官,它可保护机体免受损害,使毒物成为比较无毒的或溶解度大的物质,随胆汁或尿液排出体外。除了解毒,已经确认肝脏具有超过500种重要功能,包括产生胆汁辅助消化食物、调节凝血、平衡体内葡萄糖水平等,人只需要30%至40%左右的肝脏就可以满足正常需求,不会出现明显的症状。甚至一些患者在切除一半的肝脏后依然可以支撑起整个身体。
这本来是一件好事,但是由于肝脏的代偿能力太强大,早期肝病患者的肝功能还是正常的。而且肝脏位于腹腔,身体的内部,即使早期出现一点不舒服,往往也很难引起我们的警觉。等到有的患者出现肝脏疼痛、腹胀,消化不良,消瘦,黄疸等情况来医院看病的时候,已经是肝硬化的失代偿期了,整个肝脏的功能严重受损。90%肝癌患者是经历过“肝炎-肝硬化-肝癌”三部曲。70-90%的原发性肝癌患者都有肝硬化。肝硬化时,在肝细胞增生的过程中,可出现局灶性腺瘤样增生,易受致癌因素的作用而发生癌变,引发肝癌。
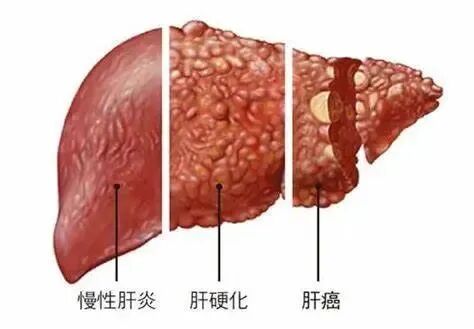
而肝脏丰富的血供可能为肿瘤生长提供了有利环境,使得肝癌容易随血液扩散转移,预后(生存)不佳。由此可见,肝硬化是肝癌的最后一道防线。及时治疗肝硬化,阻止它恶化,是预防肝癌的重要手段。
干细胞治疗肝硬化研究进展
虽然肝移植能从根本上对肝硬化进行治疗,但由于存在肝源严重匮乏和需终身服用免疫抑制剂等因素,限制了其应用。目前,临床上开展了大量干细胞治疗终末期肝病的小规模临床研究,其中研究较多且相对成熟的干细胞是间充质干细胞(mesenchymal stem cells, MSCs)。间充质干细胞存在于多种组织及器官,例如脐带组织、脐带血、胎盘、外周血等。2007年,Mohamadnejad团队最早报道了关于间充质干细胞治疗病毒性肝炎导致的终末期肝病的临床研究。

在该临床治疗中慢性乙肝感染相关的失代偿期肝硬化患者接受了间充质干细胞的治疗,患者的临床症状和生活质量明显改善,终末期肝病模型(model of end-stage liver disease, MELD)评分下降。之后国内外的一些临床治疗也发现:脐带间充质干细胞能够短期内改善终末期肝病患者的临床症状和生活质量,降低肝硬化患者肝癌的发生率和病死率。应用脐带间充质干细胞对供者和受者无额外的有创操作,且来源广泛,细胞质量可控,伦理限制较少,故目前在临床研究中应用更为广泛。
2021年11月,国内王福生院士的最新研究就使用了脐带间充质干细胞,研究结果显示,脐带间充质干细胞显著改善失代偿性肝硬化的肝功能及长期生存率。此次共有219例患者纳入研究,其中108名患者接受干细胞治疗,111名患者作为对照组,并进行了长达75个月的随访。
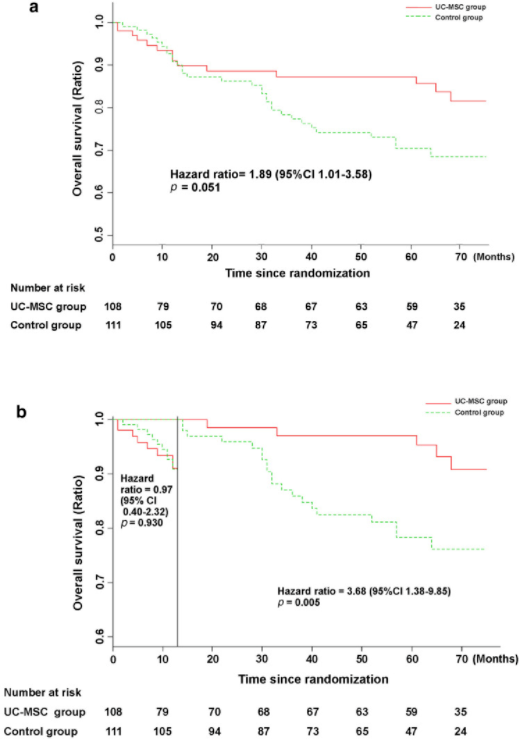
随访结果表明,脐带间充质干细胞可以减轻肝素的氨基转移,明显改善肝脏功能,并且干细胞治疗组的总体生存率高于对照组。这一研究给间充质干细胞治疗肝硬化的安全性和有效性提供了新的证据,证明了干细胞在肝硬化治疗方面展现出的良好效果。
干细胞治疗肝硬化的机制
以往认为,干细胞治疗是通过干细胞分化成肝细胞样细胞替代受损的肝细胞来改善肝功能和恢复肝脏正常结构。但随着对干细胞治疗肝病机制的进一步了解,目前认为干细胞通过旁分泌机制改变组织微环境比向肝细胞样细胞的转分化更重要。这一结果提示了间充质干细胞具有调节免疫改善肝脏炎症环境的能力。控制肝硬化的发展及恶化是预防肝癌的重要手段,而干细胞治疗或可能替代肝移植,实现受损肝脏的逆转修复。相信随着干细胞临床研究的不断深入和有序的发展,干细胞治疗肝硬化的临床应用指日可待。

干细胞是从脐带、胎盘中提取的一种修复器官机理的未完全分化的原始细胞,具有自我更新、多项分化和高度繁殖的能力,医学上称为“万能细胞”,它是形成人体各种组织器官的起源细胞。干细胞对临床上一些疑难疾病的治疗如:脑瘫、老年痴呆、脑萎缩、帕金森病、中风、肝硬化、糖尿病、红斑狼疮、股骨头坏死、软骨和关节损伤、心脏和脊髓损伤等,取得显著效果,它拥有更加鲜活细胞能量,可以快速、有效进入体内,分泌多种有益细胞因子,调节体内微环境,激活干细胞再生能力,重启时光之门,追溯青春绽放源头,实现对人体衰老状态减缓,同时有效改善身体亚健康以及预防肿瘤发生。

|
